Понимание молекулярных механизмов процессов развития - это одна из важнейших задач современной биологии. Морские ежи, относящиеся к вторичноротым животным, являются классическим объектом изучения эмбриологии, биологии развития и молекулярной биологии, поэтому в последнее время появляется все больше работ, посвященных изучению тонких механизмов их эмбриогенеза. Известно, что нормальное эмбриональное развитие этих животных связано с включением специфических сигнальных каскадов, запускаемых факторами роста через связывание с высокоафинными рецепторами. Управление ключевыми событиями в раннем развитии иглокожих (контроль миграции мезенхимных клеток, гаструляции и формирования скелета) происходит через эти сигнальные каскады. Однако работ, посвящённых изучению факторов роста и их роли в развитии морских ежей известно немного.
Классическим подходом для изучения сигнальных путей является ингибирование их отдельных компонентов. Важным инструментом для изучения взаимодействия факторов роста с их рецепторами может служить неспецифический ингибитор факторов роста сурамин (Mitrani et al., 1990; Katow, Aizu, 2002). Cурамин способен дозозависимо блокировать формирование мезодермальных структур (Mitrani et al., 1990), взаимодействуя с гепарин-связывающими факторами роста, такими как фактор роста фибробластов (FGF), фактор роста тромбоцитов (PDGF), фактор роста эндотелия сосудов (VEGF), интерлейкин 2 (Baird et al., 1988). Установлена способность сурамина предотвращать связывание PDGF со своими рецепторами на мембране фибробластов (Hosang, 1985). Другие факторы роста, например, EGF, обладают к сурамину гораздо меньшей афинностью и связываются с ним в крайне низких концентрациях (Stein, 1993).
В связи с этим, цель нашего исследования - оценить влияние неспецифического ингибирования при взаимодействии гепарин-связывающих факторов роста и их рецепторов на ход раннего развития морского ежа Strongylocentrotus intermedius.
Материалы и методы
Для определения роли каскадов реакций, запускаемых геприн-связывающими факторами роста (FGF и PDGF) в развитии морского ежа, эмбрионы Strongylocentrotus intermedius культивировали с неспецифическим ингибитором факторов роста - сурамином, а в последующих экспериментах – с сурамином и одним из факторов роста: бычьим основным FGF или человеческим PDGF-AB Факторы роста использовали в конечных концентрациях 20 нг/мл или 50 нг/мл (они были проиготовлены согласно инструкциям производителей и стерилизованы при помощи фильтрующей насадки для шприцев TPP) и добавляли одновременно с внесением сурамина. Инкубации проводили в стерильных культуральных планшетах на 24 лунки (TPP).
Статистические данные обработаны с помощью программы Statistica 6.0. Данные представлены как среднее значение ± стандартная ошибка. Полученные данные оценивали по спаренному t-критерию Стьюдента. Уровень значимости 0.05 был выбран как минимальное значение статистической разницы во всех экспериментах. Все эксперименты повторяли три раза в трёх параллелях.
Результаты
Известно, что на стадии мезенхимной бластулы у морского ежа происходит выселение клеток первичной мезенхимы в бластоцель (рис. 1, е). В дальнейшем начинается гаструляция, в ходе которой клетки вегетативного полюса втягиваются внутрь бластоцеля, при этом происходит образование архентерона (первичной кишки), со дна которого выселяются клетки вторичной мезенхимы. Во всех этих событиях участвуют сигнальные каскады, запускаемые факторами роста.
Чтобы выяснить, действительно ли сурамин блокирует пути передачи сигнала у морского ежа, нарушая взаимодействие факторов роста (FGF и PDGF) с их рецепторами, в специальной серии экспериментов мы инкубировали личинок с сурамином либо одновременно с сурамином и одним из факторов роста (FGF или PDGF). Влияние сурамина на важнейшие события в раннем эмбриогенезе морского ежа оценивали по образованию и длине архентерона, а также по индукции дифференцировки клеток первичной и вторичной мезенхимы.
Мы установили, что инкубация эмбрионов морского ежа S. intermedius с сурамином (150-300 мкМ) нарушает нормальный ход эмбрионального развития, причем эффект сурамина проявляется на определенных стадиях развития. Добавление сурамина (150-300 мкМ) на стадии зиготы не нарушало ход раннего нормального эмбрионального развития – дробление и образование морулы, формирование мезенхиной бластулы проходило в тоже время, что и в контроле, причем никаких различий между эмбрионами, инкубированными с сурамином, и эмбрионами, развитие которых шло в морской воде, нами не обнаружено (рис. 1, б-д). Однако в дальнейшем происходит заметное замедление развития, и нормальная гаструла не формируется.
Добавление сурамина на более поздней стадии развития, на стадии ранней бластулы, останавливает развитие на стадии мезенхимной бластулы: не происходит изменения формы личинки, в дальнейшем не формируются спикулы и полноценный кишечник. В некоторых случаях инкубация личинок с сурамином или с сурамином и одним из факторов роста приводит к экзогаструляции (рис. 1, л, м). Экзогаструляцию можно вызвать, добавляя к эмбрионам морских ежей хлорид лития (30 мМ), как это было описано в классических работах по изучению эмбриогенеза морских ежей (Иванова-Казас, 1978).
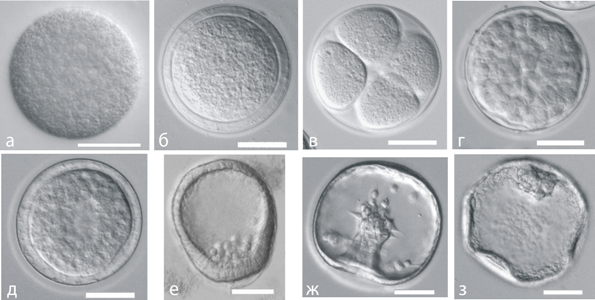
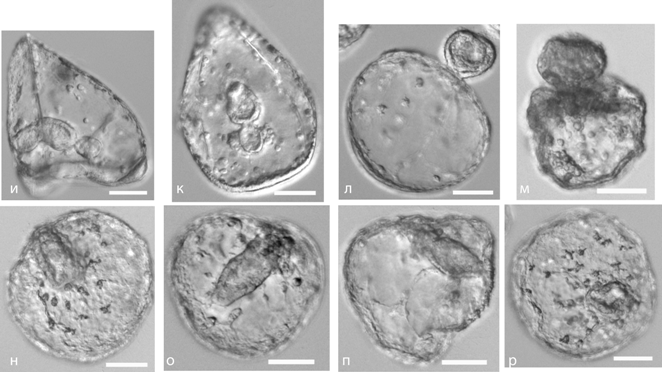
Рис. 1. Влияние сурамина и сурамина и факторов роста (FGF или PDGF) на эмбриогенез морского ежа S. intermedius. Контроль: а – яйцеклетка, б – стадия зиготы, в – стадия 4 бластомеров, г – стадия морулы, д – стадия ранней бластулы, е – мезенхимная бластула, ж – гаструла (24 ч), и, к – призма. Воздействие сурамна: з – инкубация с 300 мкМ сурамином со стадии бластулы, 24ч, л, м – экзогаструляция, вызванная сурамином (инкубация с 300 мкМ сурамином со стадии бластулы, личинкам 48 ч), н - личинка после воздействия сурамина (инкубация с 300 мкМ сурамином со стадии бластулы, личинкам 48 ч), о-р – личинки, инкубированные с сурамином (300 мкМ) и дним из факторов роста (50 нг/мл). Масштабные отрезки 50 мкм.
Установлено, что сурамин после стадии мезенхимной бластулы ингибирует образование архентерона в первой фазе его роста (1/3 длины). В то время, как в контроле эмбрионы находились на стадии средней гаструлы (высота архенторона до 1/2 всей личинки, рис. 1, ж), у эмбрионов, инкубированных с сурамином, наблюдали лишь небольшое скопление клеток на одном из полюсов (рис. 1, з). Учитывая, что первая фаза инвагинации архентерона связана с впячиванием внутрь пласта клеток с гиалиновой мембраной, а вторая фаза инвагинации связана с образованием на вершине архентерона длинных псевдоподий, которые, закрепляясь в области анимального полюса на внутренней поверхности стенки эмбриона, сокращаются и подтягивают кверху архентерон, можно говорить о том, что сурамин влияет на миграцию и перемещение клеток и клеточных полей.
На стадии поздней гаструлы (длина архентерона составляла более 2/3 от размера эмбриона) в присутствии сурамина изменения в формировании архенторона становились еще более ярко выраженными: длина архенторона была в среднем в два раза меньше, чем в контрольных личинках. На стадии призмы у некоторых личинок, инкубированных с сурамином, было зафисксировано некоторое увеличение длины архенторона (рис. 1, н, о), но, тем не менее, формирование нормального кишечника на более поздних стадиях не происходило (рис. 1 и, к).
Предполагают, что экзогенное добавление ростовых факторов при одновременном воздействии их ингибитора на эмбрионы морских ежей, может приводить к частичному нивелированию действия ингибитора (Katow, Aizu, 2002). Поэтому в следующих экспериментах мы инкубировали эмбрионы одновременно с сурамином и факторами роста (FGF или PDGF). Как мы уже указывали выше, воздействие сурамина существенно влияет на длину архентерона у личинок морского ежа, но присутствие в морской воде помимо этого ингибитора одного из исследуемых факторов сдвигает этот показатель в сторону нормы (см. рис. 2, 3). При этом разницы при использовании двух разных концентраций факторов (20 нг/мл и 50 нг/мл) мы не наблюдали. Похожую картину для сурамина и PDGF наблюдали японские исследователи (Katow, Aizu, 2002).
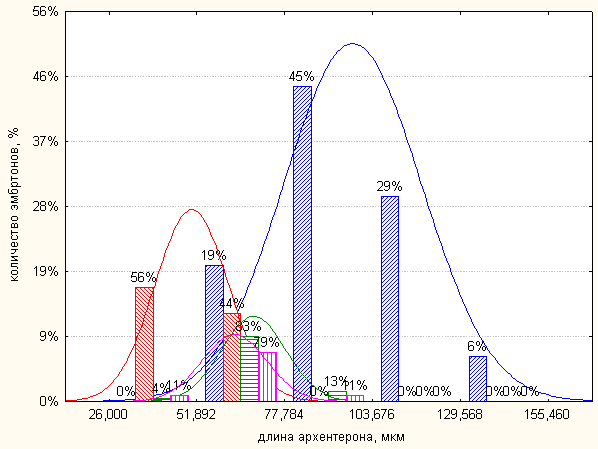
Рис. 2. Влияние 300 мкМ сурамина (красная штриховка), а также сурамина и FGF (20 нг/мл - зеленая штриховка, 50 нг/мл - розовая штриховка) на рост архентерона у эмбрионов морского ежа на стадии гаструлы. Распределение длины архентерона у контрольных эмбрионов показано синей штриховкой.
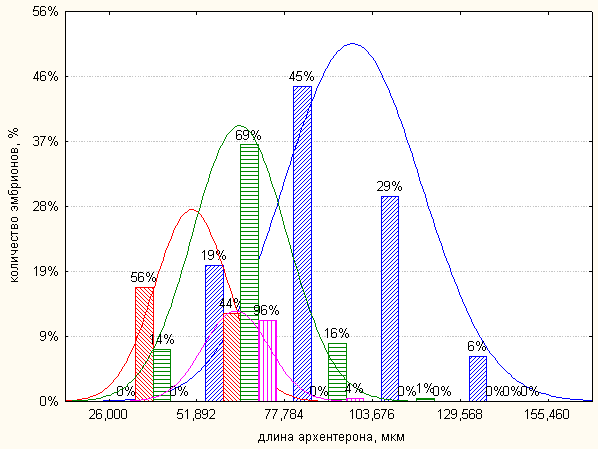
Рис. 3. Влияние 300 мкМ сурамина (красная штриховка), а также сурамина и PDGF (20 нг/мл - зеленая штриховка, 50 нг/мл - розовая штриховка) на рост архентерона у эмбрионов морского ежа на стадии гаструлы. Распределение длины архентерона у контрольных эмбрионов показано синей штриховкой.
Нами показано, что сурамин полностью блокирует образование спикул, которые необходимы для формирования личиночного скелета. Ни на каком этапе развития не удалось обнаружить спикулы ни у одной личинки (см. рис. 1 л-о). При добавлении в морскую воду помимо этого ингибитора факторов роста (FGF или PDGF) образование спикул в личинках мы также не наблюдали (см. рис. 1 п, р).
Таким образом, наши результаты показывают, что сигналы, запускаемые непосредственно FGF и PDGF, важны для миграции клеток и формирования архентерона, а также для дифференцировки клеток первичной мезенхимы. Ингибирование этих сигнальных путей нарушает ключевые события, происходящие в эмбриональном развитии морского ежа S. intermedius.
Отзыв о продукции TPP:
Криопробирки с основанием и завинчивающейся крышкой, 2,0 мл, РР, стерильные
Криопробирки были использованы для хранения разных стадий эмбрионального и личиночного развития морского ежа для последующего выделения РНК. Среди достоинств пробирок стоит отметить их удобный объём и компактный размер; устойчивость, которую им придаёт основание в форме звезды, а также тот факт, что пробирки плотно закрываются без дополнительных силиконовых уплотнений, препятствуя попаданию жидкого азота внутрь, что особенно важно для наших исследований.
Планшеты культуральные с крышкой, 24 лунки, плоское дно, 1,862 см2 (3,29 мл), PS, стерильные
Культуральные планшеты были использованы для культивирования эмбрионов морского ежа. Планшеты маркированы яркими буквами и цифрами, что позволяет быстро и легко сориентироваться и найти нужные лунки. Пластик очень прозрачный, а это важно при осмотре материала и получении фотографий.
Фильтрующая насадка для шприцев, с полиэфирсульфоновой мембраной, диаметр пор 0,22 мкм, диаметр 33 мм, стерильная
Простая в использовании и качественная насадка. Недостатков не обнаружено.
 Россия
Россия